默克知识分享|CRISPR基因编辑的机制:CRISPR簇是一个广泛存在于细菌和古生菌基因组中的特殊DNA重复序列家族,其序列由一个前导区(Leader)、多个短而高度保守的重复序列区(Repeat)和多个间隔区(Spacer)组成。
前导区一般位于CRISPR簇上游,是富含AT长度为300~500bp的区域,被认为可能是CRISPR簇的启动子序列。重复序列区长度为21~48bp,含有回文序列,可形成发卡结构。
重复序列之间被长度为26~72bp的间隔区隔开。Spacer区域由俘获的外源DNA组成,类似免疫记忆,当含有同样序列的外源DNA入侵时,可被细菌机体识别,并进行剪切使之表达沉默,达到保护自身安全的目的。
经由HDR的基因敲入
CRISPR可以利用HDR进行特定基因序列的替换和表达(敲入)。除了CRISPR的主要成分之外,HDR介导的CRISPR编辑还需要一个含有新的所需序列的DNA供体模板,其两侧是同源区域。这种供体模板的引入,连同CRISPR成分,允许细胞通过同源重组修复DSB。结果可使新序列被整合到目标基因中。
CRISPR复合体通过三个不同的步骤进行基因编辑:靶向、切割和修复。
CRISPR复合物的靶向性
根据设计,crRNA与靶DNA互补,并允许gRNA将CRISPR复合体引导到正确的基因组位置,以进行基因编辑。为了使CRISPR复合物与DNA成功结合,靶位点下游必须存在一个原间隔基邻近基序(PAM)。更多内容请到默克生命科学官网查看:www.sigmaaldrich.cn
切割DNA
一旦CRISPR复合物到达并结合目标位置,核酸酶就可以切割DNA。CRISPR复合物包含两个独立的核酸酶结构域,每个结构域切割一条特定的DNA链。HNH核酸酶结构域切割与gRNA互补的链,而RuvC核酸酶结构域负责切割非互补链。
两个核酸酶结构域协同工作,产生双链断裂(DSB),发生在PAM上游三个核苷酸处。
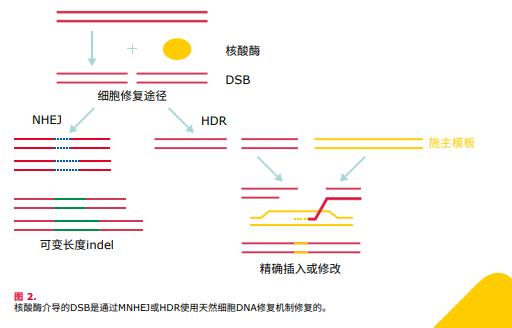
DSB的修复
一旦核酸酶切割DNA,天然的细胞DNA修复机制会试图通过以下两种机制之一来修复DSB:
非同源末端连接(NHEJ)。
同源导向修复(HDR)。
通过NHEJ进行基因敲除
NHEJ倾向于主要的细胞DSB修复机制。当DNA末端在缺乏同源DNA模板的情况下重新连接时,它会在DNA中引入插入或缺失错误(indel)
导致移码突变和过早终止密码子的Indels可以产生功能缺失(LOF)突变,这是CRISPR用于破坏(敲除)基因的主要手段。




 电话
电话
